Warum CTR-Test®?
Identifiziere unwirksame Chemotherapien vor Therapiebeginn
- Über 95% Genauigkeit bei der Identifizierung unwirksamer Chemotherapeutika vor Therapiebeginn.
- Für jeden soliden Tumor anwendbar (z.B. Eierstock, Brust, Lunge, Darm).
- Probengewinnung aus operativ entnommenem Tumorgewebe, Aszites oder Pleuraerguss möglich.
Wissenschaftlicher Erfahrungsvorsprung
- Mit 18 aussagekräftigen klinischen Studien (mit ca 2.400 untersuchten Patienten) und 11 weiteren Studien mit Tumormaterial von ca. 21.000 Patienten validiert (siehe auch Studien und Literatur).
- CTR-Test®-Ergebnisse korrelieren mit dem Therapieansprechen und dem Überleben der Patienten.
Vertrauensvoll
- Bereits 150.000 Patienten haben von dem CTR-Test® Gebrauch gemacht.
- Über 1.000 Kliniken weltweit haben den CTR-Test® bereits angewendet.
- Der CTR-Test® wird seit 2006 von TherapySelect angeboten (siehe auch Qualitätsmanagement).
Human
- Erspart den Patienten unnötige Toxizität.
- Spart wertvolle Behandlungszeit.
- Verhindert Kreuzresistenzen ansonsten wirksamer Therapien.
Kosteneffizient
- Vermeidung von Kosten durch ineffiziente Therapien.
- Vermeidet Behandlungskosten, die begleitend zur Therapie auftreten (z.B. bei Nebenwirkungen).
Was ist der CTR-Test®?
Der Krebs Therapie Response-Test (CTR-Test®) ist eine Laboruntersuchung, die vor Gabe der Chemotherapie durchgeführt wird. Dieses in vitro Diagnostikum ist in der Lage, an lebendem, operativ entnommenem Tumormaterial das Nichtansprechen (die Resistenz) von Chemotherapien für den individuellen Patienten mit sehr hoher Präzision vorherzusagen (>95%). Dies konnte in einer doppelt verblindeten, randomisierten Studie gezeigt werden. Weitere Studien belegen, dass auch der Parameter Überleben mit dem Testergebnis statistisch bedeutsam übereinstimmt und der CTR-Test® diese Variable auch beeinflussen kann.
Die hohe Genauigkeit bei der Vorhersage der Resistenz kann nur deshalb erreicht werden, weil der CTR-Test® als sehr präzise Größe das Tumorzellwachstum ausliest. Das Wachstum wird über längere Zeit in Gegenwart von den zu testenden Chemotherapeutika mit Konzentrationen, die auch im Patienten erreicht werden, ermittelt.
Für die Therapieentscheidung werden Leitlinien, Phase-III-Studienergebnisse und Zulassungsbestimmungen für die jeweiligen Chemotherapeutika herangezogen. Diese Leitlinien und Zulassungsbestimmungen ergeben sich aus der Tumorart, dem Ort der Erkrankung, dem Grad der Metastasierung, der Anzahl der Vorbehandlungen und Präferenzen des individuellen Patienten (Alter und Zustand, Nebenwirkungen vorheriger Therapien).
Nach Berücksichtigung dieser Faktoren kann die Information, welche Therapien durch den CTR-Test® als ungeeignet, da höchstwahrscheinlich unwirksam, eingestuft wurden, die Auswahl der Chemotherapeutika beeinflussen.
Eine Testdurchführung ist möglich anhand soliden Tumorgewebes, Aszites (maligner Erguss im Bauchraum) und pleuralem Erguss (maligner Erguss im Brustkorb). Nähere Informationen finden Sie auf der Seite Anwendungsbereich.
Die Medikamente, die für den CTR-Test® validiert sind, finden Sie auf der Seite Auswahl der Medikamente.
Durch die Identifikation von unwirksamen Substanzen ist es möglich, Patienten unnötige Chemotherapien und die damit verbundenen Nebenwirkungen zu ersparen. Dadurch kann auch wertvolle Behandlungszeit für andere Therapien gewonnen und die Wahrscheinlichkeit, dass sich Resistenzen gegenüber anderen Substanzen bilden (sogenannte Kreuzresistenzen), vermindert werden.
18 klinische Studien mit ca. 2.400 Patienten sind zum CTR-Test® bisher durchgeführt worden, welche auf signifikante Weise die Relevanz und den Nutzen des CTR-Tests® für den Patienten untermauern. In 11 weiteren Studien wurde der CTR-Test® mit Tumormaterial von ca. 21.000 Patienten zusätzlich validiert.
Mit ca. 150.000 durchgeführten Tests ist der CTR-Test® das führende Verfahren, um Resistenzen von Chemotherapien vor deren Applikation zu bestimmen und den Patienten die vorher als resistent identifizierten Substanzen zu ersparen. Der CTR-Test® ist damit eindeutig keine experimentelle Methode, sondern ein etabliertes Standardverfahren. Der CTR-Test® ist das weltweit am besten etablierte Verfahren zur Chemoresistenztestung und wird exklusiv von TherapySelect angeboten.
Sollten noch Fragen offen bleiben zu diesem oder anderen Themen, könnten Sie die Antwort auf der Seite FAQ zum CTR-Test finden.
 Ablauf des CTR-Tests®
Ablauf des CTR-Tests®
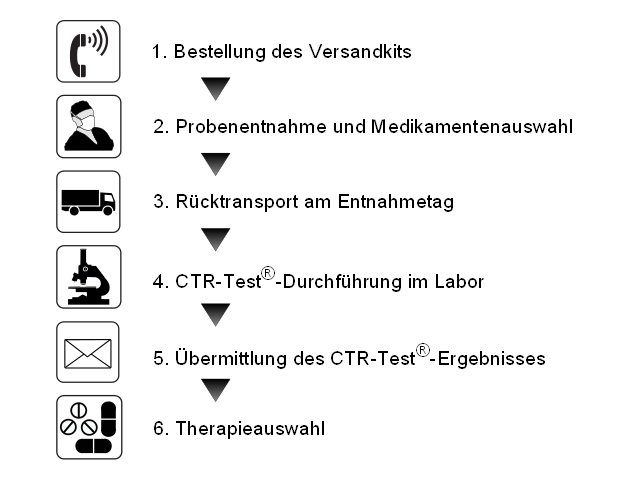
Für den Test benötigt das Labor lebendes Tumormaterial des betroffenen Patienten. Für den Transport wird ein Versandkit zur Verfügung gestellt. Das Kit sollte vor der Entnahme des Tumormaterials vor Ort sein. Der behandelnde Arzt wählt die zu testenden Medikamente aus. Direkt nach der Entnahme des Tumorgewebes wird das Tumormaterial durch einen Kurier zum Labor der TherapySelect geliefert, wo ein hoch qualifiziertes Team von Spezialisten die Tumore aufbereitet und den CTR-Test® durchführt. Das Ergebnis wird 7 - 9 Tage nach Ankunft des Tumors im Labor an den behandelnden Arzt verschickt. Der Onkologe kann nun qualifiziert die für den Patienten optimierte Tumortherapie auswählen.
Weitere Informationen zum Ablauf und zur Bestellung des CTR-Tests® finden Sie auf der Seite Ablauf und Bestellung und Dokumente zum Herunterladen.
Das CTR-Test®-Verfahren
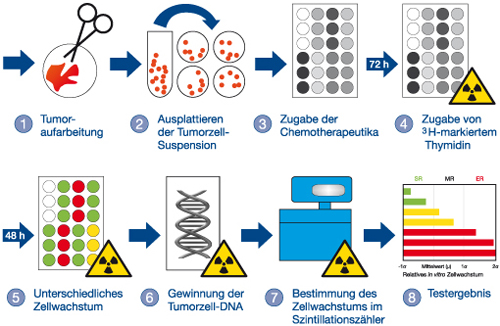
- Frisches, lebendes Tumorgewebe des jeweiligen Patienten wird zerkleinert und enzymatisch verdaut, um Tumorzellverbände (Sphäroide) zu gewinnen.
- Die Tumorzellen werden unter speziell entwickelten Bedingungen am Leben gehalten, die vorzugsweise das Wachstum von Tumorzellen begünstigen und dabei das Wachstum (möglicherweise störender) Fremdzellen unterdrücken.
- Die Tumorzellen werden dann unter sorgfältig kontrollierten Wachstumsbedingungen fünf Tage lang den zu testenden Chemotherapeutika ausgesetzt (dargestellt als farbige Punkte; unbehandelte Zellen sind weiß dargestellt).
- Tritium-markiertes Thymidin wird während der letzten 2 Tage zu den Zellen gegeben, um später das Zellwachstum bestimmen zu können.
- Nach weiteren 48 Stunden sind die Tumorzellen unterschiedlich stark gewachsen (extremes Zellwachstum, mittleres Zellwachstum, schwaches Zellwachstum).
- Die neugebildete, markierte genomische DNA wird gewonnen.
- Die Aktivität der markierten DNA wird im Szintillationszähler ausgelesen und daraus das Zellwachstum berechnet.
- Das Wachstum der chemotherapeutikabehandelten Zellen wird mit dem Wachstum der unbehandelten Kontrollgruppe (in Schritt 3 dargestellt als weiße Punkte) abgeglichen. Falls maligne Zellen, die dem Chemotherapeutikum ausgesetzt waren, im Test ähnlich stark gewachsen sind wie die der unbehandelten Gruppe, wird eine Anwendung beim Patienten mit einer Wahrscheinlichkeit von über 95% ineffizient sein. Im Testergebnis ist die Resistenz der Tumorzellen gegenüber der Chemotherapeutika an der Länge der farbigen Balken abzulesen (Extreme Resistenz, Mittlere Resistenz, Schwache Resistenz).
Das CTR-Test®-Ergebnis
Die Therapieentscheidung in Bezug auf die gewählten Chemotherapeutika, setzt sich bei rezidivierten Tumorerkrankungen aus verschiedenen Komponenten zusammen. Im Vordergrund stehen hierbei Leitlinien, Phase-III-Studienergebnisse und Zulassungsbestimmungen für die jeweiligen Chemotherapeutika. Diese Leitlinien und Zulassungsbestimmungen ergeben sich aus der Tumorart, dem Ort der Erkrankung, dem Grad der Metastasierung, der Anzahl der Vorbehandlungen und dem Staging des Patienten. Des Weiteren werden Präferenzen des individuellen Patienten berücksichtigt (Zustand des Patienten und Nebenwirkungen vorheriger Therapien).
Im Kontext dieser Informationen kann die Aussage, welche Therapien durch den CTR-Test® als ungeeignet, da mit sehr hoher Wahrscheinlichkeit (>95%) resistent, eingestuft worden sind, die Auswahl des Chemotherapeutikums beeinflussen.
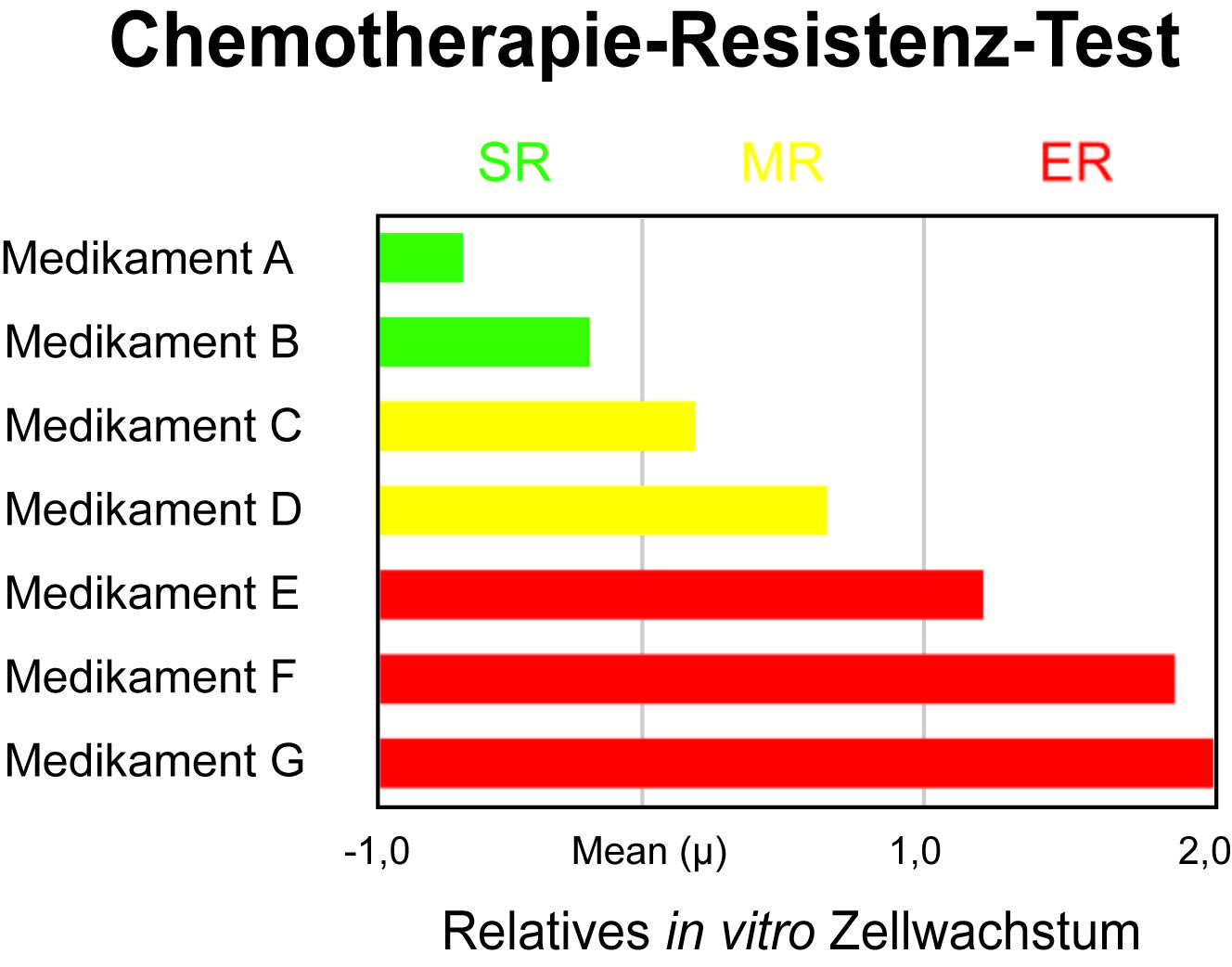
In der folgenden Grafik ist beispielhaft ein Testergebnis eines Krebspatienten dargestellt. Bei diesem Patienten wurden insgesamt sieben Medikamente getestet.
Der Tumor des Patienten zeigt eine Extreme Resistenz (ER) gegen drei Chemotherapeutika. Der Arzt kann diese inaktiven Medikamente ausschließen und damit unnötige Nebenwirkungen vermeiden. In diesem Fall kann evtl. eine alternative und wirksame Therapie verordnet werden, um den Nutzen der als wenig resistent (SR) getesteten Substanzen in Anspruch zu nehmen. Das erhöht die Chance des Patienten, eine effektive Chemotherapie zu erhalten.
|
 Klinische Bewertung des CTR-Tests®
Klinische Bewertung des CTR-Tests®
Die folgenden Informationen geben einen Überblick über die klinsche Bewertung des Tests. Eine detailiertere Übersicht finden Sie auf der Seite Studien und Literatur.
Korrelation von CTR-Test®-Ergebnis und klinischem Ansprechen
Kern & Weisenthal (1990) zeigten anhand von 450 Patienten die Beziehung zwischen dem Testergebnis (in vitro Resistenz des Patiententumors gegenüber der Chemotherapie) und dem tatsächlichen klinischen (Nicht-)Ansprechen des Patienten auf die jeweilige Chemotherapie. Ein Punkt im Graph repräsentiert jeweils eine Patientenkorrelation.
Die Patienten wurden entsprechend der CTR-Test®-Ergebnisse in 3 Gruppen (y-Achse) aufgeteilt:
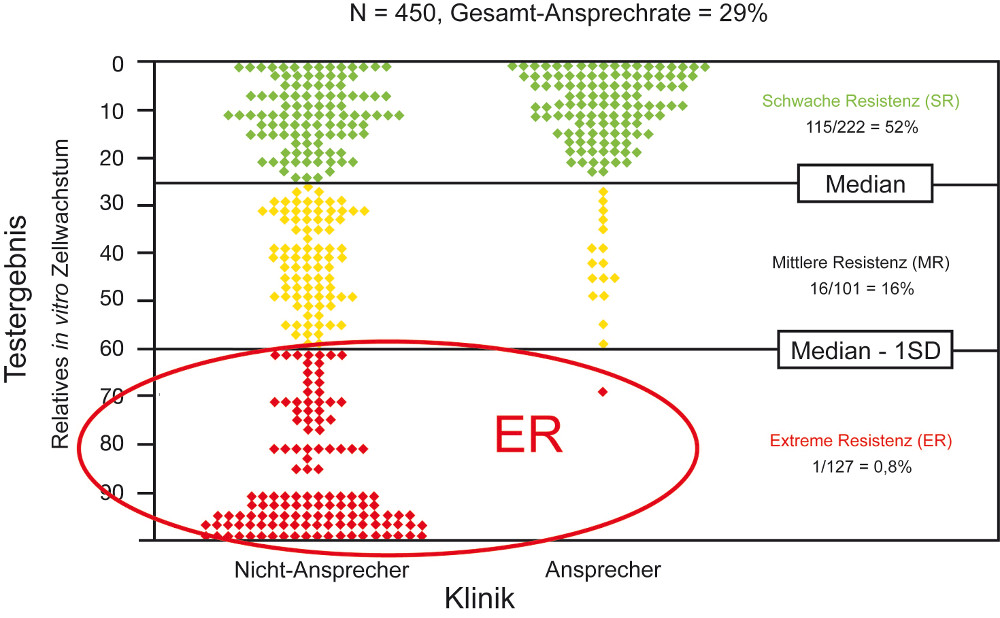
ER (Extreme Resistenz): Das Tumorzellwachstum betrug mehr als eine Standardabweichung vom Medianwert. Von 127 Patienten, deren Tumoren durch den CTR-Test® in die Kategorie der extremen Wirkstoffresistenz eingeteilt wurden, zeigten 126 (99%) kein Ansprechen auf die Chemotherapie.
MR (Mittlere Resistenz): Das Tumorzellwachstum war stärker als das mediane Wachstum, aber kleiner als eine Standardabweichung oberhalb des Medians.
SR (Schwache Resistenz): Das Tumorzellwachstum lag unter dem Medianwert. Die Tumorzellen reagierten nur wenig resistent auf das eingesetzte Medikament.
Korrelation von CTR-Test®-Ergebnis und Überlebenszeit des Patienten
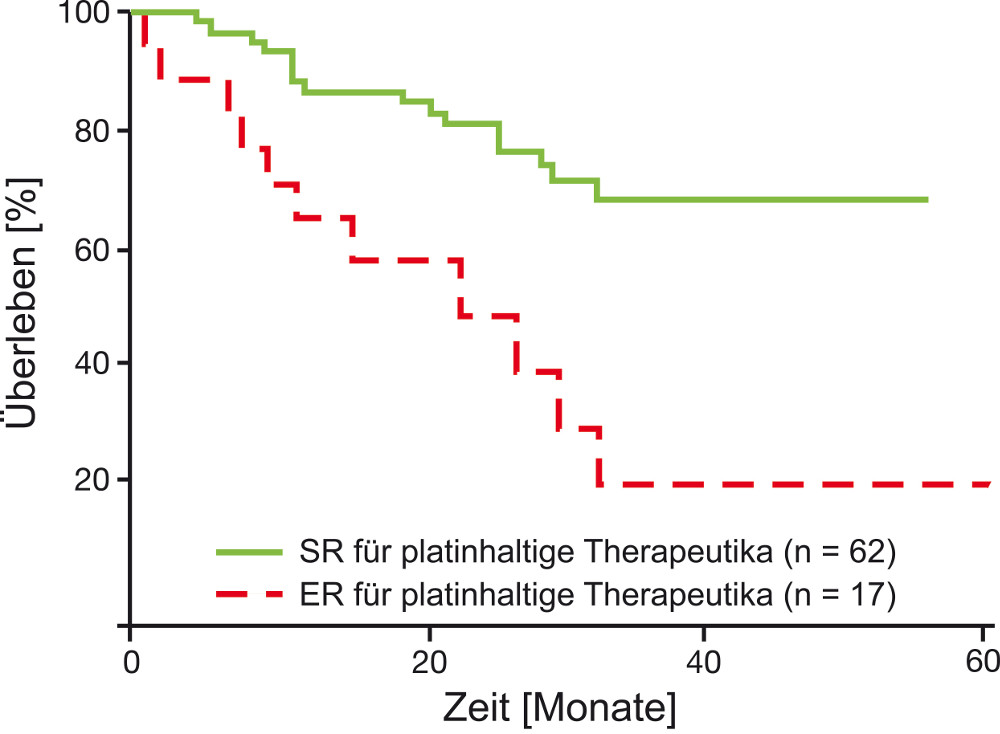
Holloway et al. (2002) zeigten, dass Patienten, deren Tumore des Eierstocks im CTR-Test® eine Platinresistenz besaßen, eine signifikant kürzere Zeit bis zum Wiederauftreten des Tumors und eine geringere Überlebensdauer aufzeigten, wenn sie mit platinhaltigen Chemotherapeutika behandelt worden waren (p=0,0003).
Ähnliches konnte für Brustkrebs-Patientinnen bei der Gabe von Kombinationschemotherapien gezeigt werden.
Verlängerung der Überlebenszeit durch CTR-Test®-Ergebnis dirigierte Chemotherapie
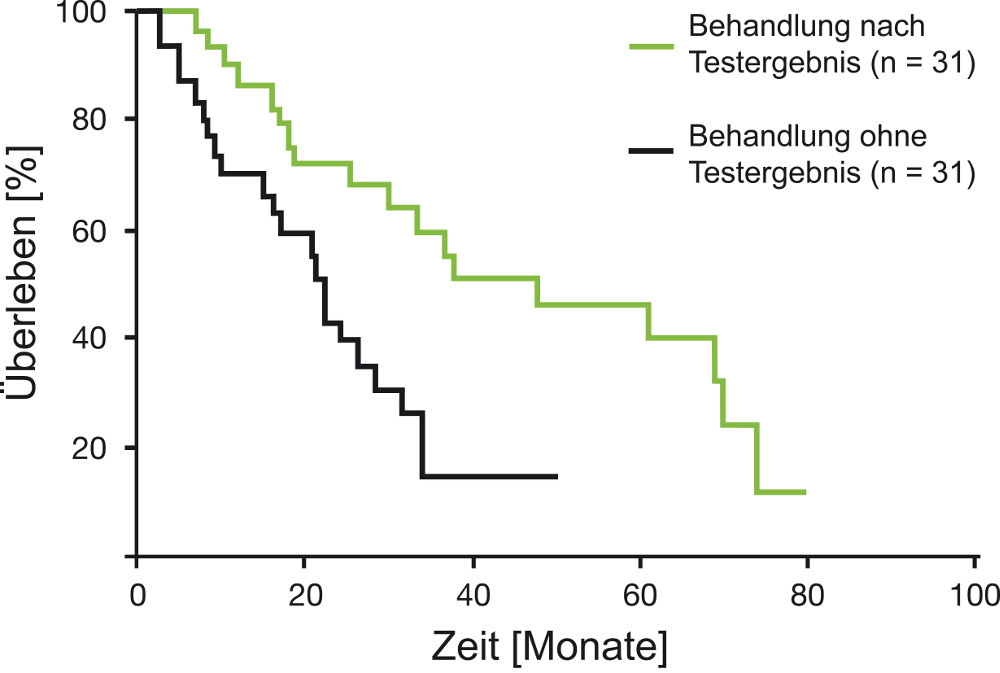
Loizzi et al. (2003), zeigten in einer klinischen Studie am platinsensitiven epithelialen Ovarialkarzinom, dass die mediane Überlebenszeit von Eierstockkrebs-Patientinnen im Rezidivfall durch eine nach dem Testergebnis gestaltete Behandlung um 81% verlängert werden konnte. Das progressionsfreie Einjahresüberleben betrug 90% für die Gruppe, die nach dem Testergebnis behandelt wurde, verglichen mit 70% in der Kontrollgruppe (Behandlung ohne Testergebnis) (p=0,005).
Prospektiv randomisierte Studie zum Platin-Therapieansprechen beim primären Ovarialkarzinom
Verleye et al. (Okt 2008) zeigten im Rahmen der EORTC Studie 55971 an 246 primären Ovarialkarzinom-Patientinnen in einem prospektiven, randomisierten, doppeltverblindeten Testdesign, dass in vitro Platinresistenz im CTR-Test® gut mit klinischem Therapieversagen der Platin Chemotherapie korreliert (p = 0,008). Dadurch ist gezeigt, dass Resistenzvorhersage für Carboplatin mit Hilfe des CTR-Tests® ein unabhängiger signifikanter prädiktiver Faktor für die Vorhersage von Therapieversagen bei der Erstbehandlung mit platinbasierten Chemotherapien beim fortgeschrittenen Ovarialkarzinom ist.
Erfahren Sie mehr dazu:




